Los hidrocarburos aromáticos , son hidrocarburos cíclicos, llamados así
debido al fuerte aroma que caracteriza a la mayoría de ellos, se consideran
compuestos derivados del benceno, pues la estructura cíclica del benceno se encuentra presente en
todos los compuestos aromáticos.
Existen muchas formas de
representar al Benceno, por ejemplo la fórmula desarrollada (1),
la estructura de Kekulé (2) o el modelo de anillo (3):
PROPIEDADES




http://es.slideshare.net/WeezyRealg/reporte-prctica-3
http://www.quimicas.net/2015/05/ejemplos-de-hidrocarburos-aromaticos.html
http://www.quimicaorganica.org/benceno/problemas-nomenclatura-benceno/299-nomenclatura-de-benceno-reglas-iupac.html
El nombre genérico de los hidrocarburos
aromáticos mono y policíclicos es "areno" y los radicales
derivados de ellos se llaman radicales "arilo". Todos ellos se
pueden considerar derivados del benceno, que es una molécula cíclica,
de forma hexagonal y con un orden de enlace intermedio entre un enlace sencillo
y un doble enlace. Experimentalmente se comprueba que los seis enlaces son
equivalentes, de ahí que la molécula de benceno se represente como una
estructura resonante entre las dos fórmulas propuestas por Kekulé, en 1865,
según el siguiente esquema:
Cuando el benceno lleva un radical se
nombra primero dicho radical seguido de la palabra "-benceno".
Si son dos los radicales se indica su
posición relativa dentro del anillo bencénico mediante los números 1,2; 1,3 ó
1,4, teniendo el número 1 el sustituyente más importante. Sin embargo, en estos
casos se sigue utilizando los prefijos "orto", "meta" y
"para" para indicar esas mismas posiciones del segundo
sustituyente.
En el caso de haber más de dos
sustituyentes, se numeran de forma que reciban los localizadores más
bajos, y se ordenan por orden alfabético. En caso de que haya varias opciones
decidirá el orden de preferencia alfabético de los radicales. 1-etil-2,5-dimetil-4-propilbenceno
Cuando el benceno actúa como radical de
otra cadena se utiliza con el nombre de "fenilo". 4-etil-1,6-difenil-2-metilhexano
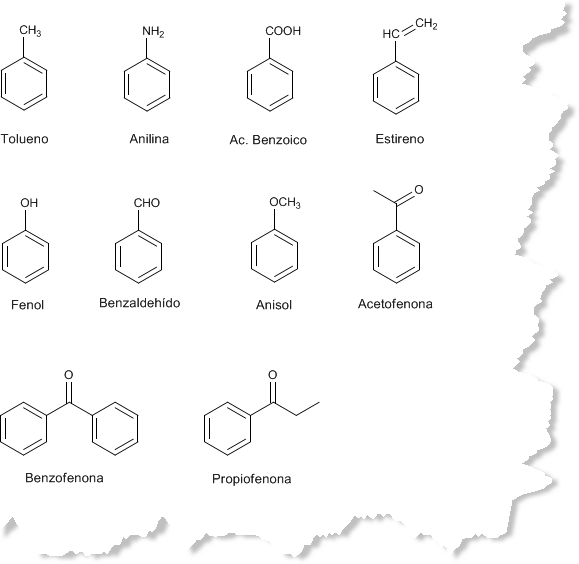
Existen
numerosos derivados del benceno con nombres comunes que conviene saber:
El benceno tiene un punto de fusión de
5,5 °C, un punto de ebullición de 80,1 °C, y una densidad relativa
de 0,88 a 20 °C.Es un líquido incoloro de olor agradable (aroma dulce).
Son conocidos sus efectos cancerígenos,
y puede resultar venenoso si se inhala en grandes cantidades. Sus vapores son
explosivos, y el líquido es violentamente inflamable. A partir del benceno se
obtienen numerosos compuestos, como el nitrobenceno. También es empleado en la
producción de medicinas y de otros derivados importantes como la anilina y el
fenol. El benceno y sus derivados se encuentran incluidos en el grupo químico
conocido como compuestos aromáticos.
El benceno puro arde con una llama
humeante debido a su alto contenido de carbon.
Mezclado con grandes proporciones de gasolina constituye un combustible
aceptable. En Europa era
frecuente añadir al benceno mezclado con tolueno y otros compuestos asociados
al combustible de los motores, y
sólo recientemente se ha tenido en cuenta su condición de agente cancerígeno.
REACCIONES DE LOS HIDROCARBUROS AROMÁTICOS
1.- Sustitución electrofílica aromática. Constituye la reacción más característica del anillo aromático. Dependiendo del electrófilo que se incorpora al anillo aromáticos tenemos:
a) Halogenación.
b) Nitración.
a) Sulfonación.
b) Alquilación de Friedel.Crafts.
c)
Acilación de Friedel-Crafts.
d) Reacciones de derivados del benceno (Efecto de la orientación).En las reacciones de los derivados bencénicos la posición donde reacciona el electrófilo vendrá determinada por el carácter del grupo ya presente en el anillo aromático y que resumimos a continuación:Carácter activante y orientador orto-para : -R; -OR; -OH; -NR2 y – O-.Carácter desactivante y orientador meta : -NO2; -SO3H; -NR+3 y –CO-R.Carácter desactivante y orientador orto-para : -Cl; -Br; -I. Además hay que tener en cuenta el efecto estérico del grupo sobre el anillo aromático.
2.- Reacciones de adición.
b) Hidrogenación.
c) Reacción de Birch.
3.- Reacciones de los alquilbencenos.
Ensayos de aromaticidad
a. Reacción de Friedel-Crafts. Hidrocarburos aromáticos derivados del benceno y sus análogos
halogenados reaccionan con cloroformo en presencia de tricloruro de aluminio anhidro para producir
colores, dependiendo de la complejidad del anillo sobre el cloruro de aluminio sublimado. Si fuese un
benceno, el producto principal de la reacción Friedel- Crafts es el trifenilmetano, que en solución como
sales del AlCl4 dan coloración.
C6H6
benceno
CHCl3
AlCl3
(C6H5
)3CH 3 HCl
trifenilmetano
Compuestos no aromáticos que contienen bromo producen color amarillo y alquenos que contienen
yodo producen color violeta; si es un derivado del benceno, color anaranjado (a rojo); si es un naftaleno,
de color azul; si es un fenantreno da color púrpura y si es antraceno da color verde. Con el tiempo los
colores de todos cambian a tono café. Si el aromático tiene sustituyentes desactivantes, como el grupo
nitro, no dan coloración. ( Lozano.L, Romero. A, Urbina.J.manual practica de laboratorio I de quimica organica)
b. Ensayo de formaldehído - ácido sulfúrico. Este test es utilizado para diferenciar compuestos
aromáticos de los no aromáticos de sustancias que han sido insolubles en ácido sulfúrico concentrado. La
reacción del formaldehído con ácido sulfúrico genera electrófilos reactivos de tipo +CH2OH que con el
núcleo aromático polimerizan, generando en la solución coloraciones en la capa superior al añadir el
compuesto. Los colores típicos observados en este test son: para benceno, tolueno y n-butilbenceno
coloración roja, sec-butilbenceno coloración rosada, tert-butilbenceno y mesitileno color naranja, difenil- y trifenilbenceno color azul y verde azulado, haluros de arilo color rosado o púrpura, naftil éter color
púrpura. Algunos cicloalcanos y sus derivados halogenados podrían mostrar un color amarillo pálido o no
dar coloración y muchos de ellos precipitan. La mayoría de los compuestos que dan el ensayo positivo, el
color cambia entre gris y negro. La reacción es inhibida por grupos sustituyentes que atraen electrones
desactivando el anillo como –Cl, -SO3H, -NO2
, -COOH, -CH2
-N
+
(R)3
. ( Lozano.L, Romero. A, Urbina.J.manual practica de laboratorio I de quimica organica)
BIBLIOGRAFIA
https://www.clubensayos.com/Ciencia/LABORATORIO-4-COMPUESTOS-AROMATICOS/1153264.html
http://es.slideshare.net/WeezyRealg/reporte-prctica-3
http://www.quimicas.net/2015/05/ejemplos-de-hidrocarburos-aromaticos.html
http://www.quimicaorganica.org/benceno/problemas-nomenclatura-benceno/299-nomenclatura-de-benceno-reglas-iupac.htm
http://www.rochester.edu.co/ckfinder/uploads/files/DIEGO-M-QUIMICA%2011/manual%20de%20practicas%20de%20laboratorio%20UIS.pdf
Existen muchas formas de representar al Benceno, por ejemplo la fórmula desarrollada (1), la estructura de Kekulé (2) o el modelo de anillo (3):
PROPIEDADES


 | ||
 | ||
 | |||
http://www.quimicas.net/2015/05/ejemplos-de-hidrocarburos-aromaticos.html
http://www.quimicaorganica.org/benceno/problemas-nomenclatura-benceno/299-nomenclatura-de-benceno-reglas-iupac.html
Cuando el benceno lleva un radical se
nombra primero dicho radical seguido de la palabra "-benceno".
Si son dos los radicales se indica su posición relativa dentro del anillo bencénico mediante los números 1,2; 1,3 ó 1,4, teniendo el número 1 el sustituyente más importante. Sin embargo, en estos casos se sigue utilizando los prefijos "orto", "meta" y "para" para indicar esas mismas posiciones del segundo sustituyente.
Si son dos los radicales se indica su posición relativa dentro del anillo bencénico mediante los números 1,2; 1,3 ó 1,4, teniendo el número 1 el sustituyente más importante. Sin embargo, en estos casos se sigue utilizando los prefijos "orto", "meta" y "para" para indicar esas mismas posiciones del segundo sustituyente.
Cuando el benceno actúa como radical de
otra cadena se utiliza con el nombre de "fenilo". 4-etil-1,6-difenil-2-metilhexano
Existen
numerosos derivados del benceno con nombres comunes que conviene saber:

El benceno tiene un punto de fusión de
5,5 °C, un punto de ebullición de 80,1 °C, y una densidad relativa
de 0,88 a 20 °C.Es un líquido incoloro de olor agradable (aroma dulce).
Son conocidos sus efectos cancerígenos,
y puede resultar venenoso si se inhala en grandes cantidades. Sus vapores son
explosivos, y el líquido es violentamente inflamable. A partir del benceno se
obtienen numerosos compuestos, como el nitrobenceno. También es empleado en la
producción de medicinas y de otros derivados importantes como la anilina y el
fenol. El benceno y sus derivados se encuentran incluidos en el grupo químico
conocido como compuestos aromáticos.
El benceno puro arde con una llama
humeante debido a su alto contenido de carbon.
Mezclado con grandes proporciones de gasolina constituye un combustible
aceptable. En Europa era
frecuente añadir al benceno mezclado con tolueno y otros compuestos asociados
al combustible de los motores, y
sólo recientemente se ha tenido en cuenta su condición de agente cancerígeno.
REACCIONES DE LOS HIDROCARBUROS AROMÁTICOS
1.- Sustitución electrofílica aromática. Constituye la reacción más característica del anillo aromático. Dependiendo del electrófilo que se incorpora al anillo aromáticos tenemos:
a) Halogenación.
b) Nitración.
a) Sulfonación.
b) Alquilación de Friedel.Crafts.
Recordar que como la reacción de alquilación tiene lugar a través de carbocationes se pueden producir transposiciones.
c)
Acilación de Friedel-Crafts.
d) Reacciones de derivados del benceno (Efecto de la orientación).En las reacciones de los derivados bencénicos la posición donde reacciona el electrófilo vendrá determinada por el carácter del grupo ya presente en el anillo aromático y que resumimos a continuación:Carácter activante y orientador orto-para : -R; -OR; -OH; -NR2 y – O-.Carácter desactivante y orientador meta : -NO2; -SO3H; -NR+3 y –CO-R.Carácter desactivante y orientador orto-para : -Cl; -Br; -I. Además hay que tener en cuenta el efecto estérico del grupo sobre el anillo aromático.
2.- Reacciones de adición.
a) Cloración.
b) Hidrogenación.
c) Reacción de Birch.
3.- Reacciones de los alquilbencenos.
a) Oxidación.
Recordar que para que la oxidación se lleve a cabo debe de haber un hidrógeno sobre el carbono bencílico.
b) Halogenación.
c) Reducción de acilbencenos a alquilbencenos (Reducción de Clemmensen).
4.- Reacciones de los alquenilbencenos. Cuando sobre el anillo aromático tenemos una cadena insaturada (doble enlace), hay que tener en cuenta que entonces tendremos dos centros de reacción, uno será el anillo aromático y otro el doble enlace. En condiciones normales el primero en reaccionar para las reacciones de adición será el doble enlace ya que la reacción sobre al anillo aromático requiere condiciones más enérgicas al estar estabilizado por resonancia. Por ello podemos decir que los alquenilbencenos experimentan reacciones de sustitución en el anillo y de adición en la cadena.
5.- Sustitución nucleófilica aromática. Los nucleófilos desplazan fácilmente a los iones haluro de los haluros de arilo cuando hay grupos atrayentes de electrones (desactivantes) en las posiciones orto ó para con respecto al haluro.
PRACTICA SUGERIDA EN LABORATORIO
Ensayos de aromaticidad a. Reacción de Friedel-Crafts. Hidrocarburos aromáticos derivados del benceno y sus análogos halogenados reaccionan con cloroformo en presencia de tricloruro de aluminio anhidro para producir colores, dependiendo de la complejidad del anillo sobre el cloruro de aluminio sublimado. Si fuese un benceno, el producto principal de la reacción Friedel- Crafts es el trifenilmetano, que en solución como sales del AlCl4 dan coloración. C6H6 benceno CHCl3 AlCl3 (C6H5 )3CH 3 HCl trifenilmetano Compuestos no aromáticos que contienen bromo producen color amarillo y alquenos que contienen yodo producen color violeta; si es un derivado del benceno, color anaranjado (a rojo); si es un naftaleno, de color azul; si es un fenantreno da color púrpura y si es antraceno da color verde. Con el tiempo los colores de todos cambian a tono café. Si el aromático tiene sustituyentes desactivantes, como el grupo nitro, no dan coloración. ( Lozano.L, Romero. A, Urbina.J.manual practica de laboratorio I de quimica organica)
b. Ensayo de formaldehído - ácido sulfúrico. Este test es utilizado para diferenciar compuestos aromáticos de los no aromáticos de sustancias que han sido insolubles en ácido sulfúrico concentrado. La reacción del formaldehído con ácido sulfúrico genera electrófilos reactivos de tipo +CH2OH que con el núcleo aromático polimerizan, generando en la solución coloraciones en la capa superior al añadir el compuesto. Los colores típicos observados en este test son: para benceno, tolueno y n-butilbenceno coloración roja, sec-butilbenceno coloración rosada, tert-butilbenceno y mesitileno color naranja, difenil- y trifenilbenceno color azul y verde azulado, haluros de arilo color rosado o púrpura, naftil éter color púrpura. Algunos cicloalcanos y sus derivados halogenados podrían mostrar un color amarillo pálido o no dar coloración y muchos de ellos precipitan. La mayoría de los compuestos que dan el ensayo positivo, el color cambia entre gris y negro. La reacción es inhibida por grupos sustituyentes que atraen electrones desactivando el anillo como –Cl, -SO3H, -NO2 , -COOH, -CH2 -N + (R)3 . ( Lozano.L, Romero. A, Urbina.J.manual practica de laboratorio I de quimica organica)
Ensayos de aromaticidad a. Reacción de Friedel-Crafts. Hidrocarburos aromáticos derivados del benceno y sus análogos halogenados reaccionan con cloroformo en presencia de tricloruro de aluminio anhidro para producir colores, dependiendo de la complejidad del anillo sobre el cloruro de aluminio sublimado. Si fuese un benceno, el producto principal de la reacción Friedel- Crafts es el trifenilmetano, que en solución como sales del AlCl4 dan coloración. C6H6 benceno CHCl3 AlCl3 (C6H5 )3CH 3 HCl trifenilmetano Compuestos no aromáticos que contienen bromo producen color amarillo y alquenos que contienen yodo producen color violeta; si es un derivado del benceno, color anaranjado (a rojo); si es un naftaleno, de color azul; si es un fenantreno da color púrpura y si es antraceno da color verde. Con el tiempo los colores de todos cambian a tono café. Si el aromático tiene sustituyentes desactivantes, como el grupo nitro, no dan coloración. ( Lozano.L, Romero. A, Urbina.J.manual practica de laboratorio I de quimica organica)
b. Ensayo de formaldehído - ácido sulfúrico. Este test es utilizado para diferenciar compuestos aromáticos de los no aromáticos de sustancias que han sido insolubles en ácido sulfúrico concentrado. La reacción del formaldehído con ácido sulfúrico genera electrófilos reactivos de tipo +CH2OH que con el núcleo aromático polimerizan, generando en la solución coloraciones en la capa superior al añadir el compuesto. Los colores típicos observados en este test son: para benceno, tolueno y n-butilbenceno coloración roja, sec-butilbenceno coloración rosada, tert-butilbenceno y mesitileno color naranja, difenil- y trifenilbenceno color azul y verde azulado, haluros de arilo color rosado o púrpura, naftil éter color púrpura. Algunos cicloalcanos y sus derivados halogenados podrían mostrar un color amarillo pálido o no dar coloración y muchos de ellos precipitan. La mayoría de los compuestos que dan el ensayo positivo, el color cambia entre gris y negro. La reacción es inhibida por grupos sustituyentes que atraen electrones desactivando el anillo como –Cl, -SO3H, -NO2 , -COOH, -CH2 -N + (R)3 . ( Lozano.L, Romero. A, Urbina.J.manual practica de laboratorio I de quimica organica)
BIBLIOGRAFIA
https://www.clubensayos.com/Ciencia/LABORATORIO-4-COMPUESTOS-AROMATICOS/1153264.html
http://es.slideshare.net/WeezyRealg/reporte-prctica-3
http://www.quimicas.net/2015/05/ejemplos-de-hidrocarburos-aromaticos.html
http://www.quimicaorganica.org/benceno/problemas-nomenclatura-benceno/299-nomenclatura-de-benceno-reglas-iupac.htm
http://www.rochester.edu.co/ckfinder/uploads/files/DIEGO-M-QUIMICA%2011/manual%20de%20practicas%20de%20laboratorio%20UIS.pdfhttp://es.slideshare.net/WeezyRealg/reporte-prctica-3
http://www.quimicas.net/2015/05/ejemplos-de-hidrocarburos-aromaticos.html
http://www.quimicaorganica.org/benceno/problemas-nomenclatura-benceno/299-nomenclatura-de-benceno-reglas-iupac.htm















